Caro-Teller JM, Cortijo-Cascajares S, Escribano-Valenciano I, Campo-Angora M, Ferrari-Piquero JM
Servicio de Farmacia. Hospital Universitario 12 de Octubre. Madrid (España)
____
Rev. OFIL 2016, 26;2:117-122
Fecha de recepción: 08/06/2015 – Fecha de aceptación: 03/01/2016
____
Resumen
Objetivos: Identificar, describir y establecer recomendaciones terapéuticas para las interacciones farmacológicas entre abiraterona y la medicación concomitante de pacientes con cáncer de próstata metastásico.
Material y métodos: Estudio observacional descriptivo retrospectivo que incluye todos los pacientes tratados con abiraterona durante el año 2014. Se registraron edad y medicación domiciliaria concomitante. Las interacciones se identificaron utilizando la herramienta Lexi-InteractTM y se clasificaron en tres categorías (leve, moderada y grave) según su relevancia clínica. Se analizó el mecanismo de acción de cada interacción y se determinaron los fármacos más implicados. Se establecieron las siguientes recomendaciones generales: monitorizar el tratamiento (para las interacciones leves), considerar la sustitución terapéutica (para las moderadas) y evitar la asociación (para las graves).
Resultados: Se incluyeron 38 pacientes. La mediana del número de fármacos administrados concomitantemente fue 10 (rango: 2-17). Se registraron 90 interacciones con abiraterona, pertenecientes a 43 fármacos diferentes. El 81,58% de los pacientes presentó al menos una interacción potencial. La mediana de interacciones por paciente fue 2 (rango: 0-6). La distribución de las interacciones en función de su relevancia fue: 65 leves (72,22%), 22 moderadas (24,44%) y 3 graves (3,34%). Los principales mecanismos de acción de las interacciones detectadas se basaron en la inhibición por abiraterona del CYP3A4 (28,6%), CYP2D6 (16,7%), CYP2C9 (11,9%) y de la glicoproteína-P (21,4%).
Conclusiones: La mayor parte de los pacientes presentaron al menos una interacción potencial entre su tratamiento domiciliario y abiraterona. Las interacciones analizadas se deben principalmente al efecto inhibidor de abiraterona sobre múltiples vías de metabolización.
Palabras clave: Abiraterona, próstata, interacción.
____
Correspondencia:
José Manuel Caro-Teller
C/ Uruguay, 8 – 10º D
28822 Coslada (Madrid)
Correo electrónico: josemanuel.caro@hotmail.com
____
Introducción
El cáncer de próstata es el más frecuente en la población masculina occidental, con 27.853 casos nuevos en España en 2012 lo que supone un 12,9% del total de cánceres diagnosticados. En la población general, es la quinta neoplasia maligna con mayor mortalidad y la tercera entre la población masculina (5.481 casos en 2012)1.
Así como en su momento los taxanos supusieron un cambio de paradigma en el tratamiento del cáncer de próstata; el descubrimiento de la síntesis de andrógenos de origen extratesticular por las propias células cancerosas, ha dado lugar a la investigación de una nueva generación de fármacos antiandrogénicos que están proporcionando una nueva estrategia terapéutica para esta enfermedad. El primer agente comercializado de este grupo es el acetato de abiraterona, cuyo mecanismo de acción se basa en su potente, selectiva e irreversible capacidad inhibidora de la enzima 17α-hidroxilasa/C17,20-liasa (CYP17); la cual cataliza la conversión de pregnenolona y progesterona a dehidroepiandrosterona (DHEA) y androstenodiona respectivamente2. Esta enzima es fundamental para la síntesis de andrógenos en testículos, glándulas suprarrenales y tejidos prostáticos tumorales. Con la inhibición en una fase tan temprana se reducen los niveles de testosterona a valores nanomolares3.
Abiraterona es una molécula con una formulación oral que si originalmente fue aprobada por las agencias reguladoras para el tratamiento del cáncer de próstata metastásico resistente a la castración (CPRCm) que han progresado a un régimen basado en taxanos, en la actualidad su indicación se ha ampliado a pacientes asintomáticos o levemente sintomáticos en los cuales la quimioterapia aún no está clinicamente indicada4. La ampliación de su indicación ha permitido que especialidades médicas como Oncología Radioterápica y Urología puedan prescribirlo bajo los criterios indicados, sin necesidad de que el paciente sea derivado al oncólogo.
Los avances diagnósticos, quirúrgicos y farmacológicos han permitido que la supervivencia de los pacientes con cáncer de próstata haya aumentado sustancialmente en los últimos años, tanto que en la actualidad, la supervivencia de la enfermedad a los 5 años es del 76-80% para todos los estadíos en global5. La larga supervivencia junto con el envejecimiento de la población, nos lleva a un escenario en el que dos tercios de los pacientes con cáncer de próstata son mayores de 65 años. Por tanto, la mayoría de los pacientes subsidiarios de recibir tratamiento con abiraterona, son varones de edad media o avanzada; generalmente con tratamientos concomitantes para patologías crónicas de base.
La polimedicación aumenta la probabilidad de que aparezca una interacción farmacológica (IF). Se define IF como la influencia que un fármaco ejerce sobre otro cuando se administran juntos, desencadenando un cambio cualitativo o cuantitativo en sus efectos6. Se estima que el riesgo potencial de sufrir una IF es del 70% en pacientes que toman cinco fármacos al mismo tiempo y asciende a un 100% si se toman siete7. Dichas IF pueden ser meramente teóricas sin consecuencias clínicas para el paciente o llegar a desencadenar procesos graves8. Unas IF muy relevantes son las que varían los niveles plasmáticos de fármaco: un aumento de los niveles plasmáticos puede generar una toxicidad excesiva y una disminución muy problablemente conllevará una respuesta terapéutica insuficiente6. En el caso de los antineoplásicos orales, la repercusión de una IF puede ser trascendental, ya que si tiene la relevancia suficiente puede llevar al fracaso del tratamiento y tener impacto incluso en la supervivencia de los pacientes9.
El presente estudio tiene como objetivo identificar, describir y establecer recomendaciones terapéuticas para las interacciones farmacológicas entre abiraterona y la medicación concomitante de pacientes con cáncer de próstata metastásico.
Material y métodos
Estudio observacional descriptivo retrospectivo que incluye a todos los pacientes con cáncer de próstata tratados con abiraterona en un hospital de tercer nivel durante el año 2014. Se registró la edad y la medicación domiciliaria de cada paciente durante su tratamiento con abiraterona. Para ello se utilizó la aplicación informática HORUS®. Se trata del Sistema del historial médico electrónico de la Comunidad de Madrid que está a disposición de todos los facultativos de Centros de Salud y Hospitales con el objetivo de facilitar el acceso a la información médica y farmacológica de los pacientes.
Las IF potenciales fueron detectadas utilizando la herramienta Lexi-InteractTM y se clasificaron en tres categorías según su gravedad (leve, moderada y grave).
Se analizó el mecanismo de acción de cada interacción y se relacionó con los fármacos implicados en cada una de ellas. Se establecieron unas recomendaciones generales en función de la trascendencia de las interacciones detectadas: monitorizar el tratamiento (para las interacciones leves), considerar la sustitución terapéutica (para las moderadas) y evitar la asociación (para las graves).
Resultados
Durante el periodo del estudio se incluyeron un total de 38 pacientes con cáncer de próstrata tratados con abiraterona, con una media de edad de 75±9,2 años. La mediana del número de fármacos administrados concomitantemente fue 10 (rango: 2-17).
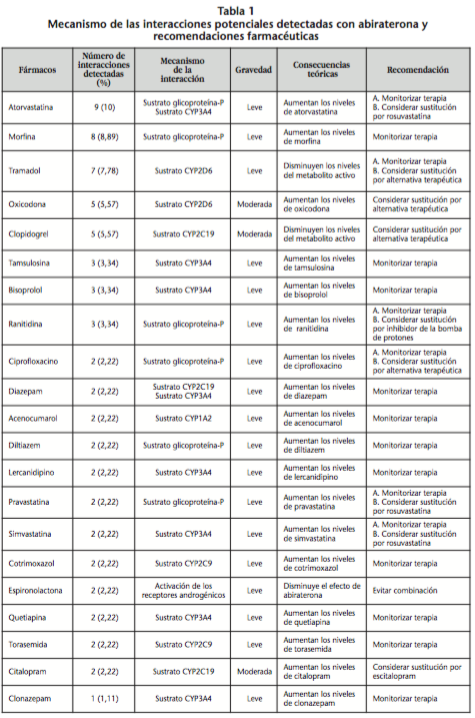
Se registraron un total de 90 interacciones potenciales con abiraterona, pertenecientes a 43 fármacos diferentes. 31 pacientes (81,58%) presentaron al menos una interacción potencial con abiraterona. La mediana de interacciones por paciente fue 2 (rango: 0-6). Los fármacos más frecuentemente implicados en dichas interacciones por orden decreciente fueron: atorvastatina (10%), morfina (8,89%), tramadol (7,78%), oxicodona (5,57%), clopidogrel (5,57%), tamsulosina (3,34%), bisoprolol (3,34%) y ranitidina (3,34%).
De las 90 interacciones potenciales detectadas, su distribución en función de su gravedad fue: 65 de carácter leve (72,22%), 22 de carácter moderado (24,44%) y 3 de carácter grave (3,34%).
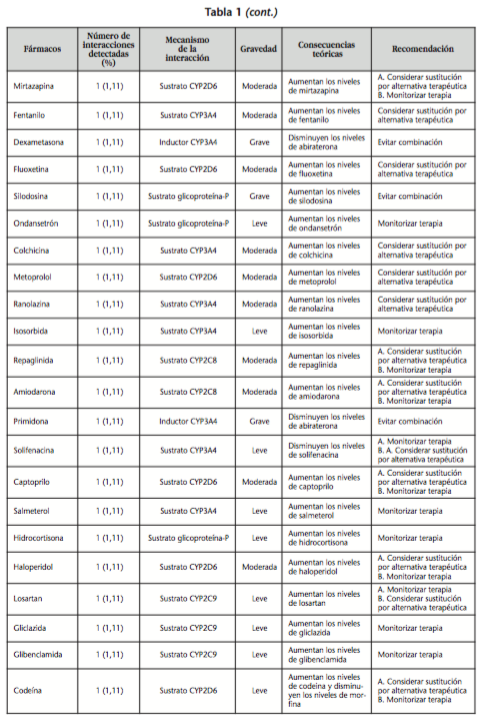
En las interacciones registradas, el principal mecanismo de acción implicado se basó en el efecto inhibidor de acetato de abiraterona sobre múltiples enzimas metabolizadoras hepáticas como CYP3A4 (31,1%), CYP2D6 (17,8%), CYP2C9 (11,1%), CYP2C19 (6,7%), CYP2C8 (4,4%) y CYP1A2 (2,2%). La inhibición por abiraterona de la glicoproteína-P (proteína transportadora de fármacos dependiente de energía) fue el segundo mecanismo más implicado en el desarrollo de interacciones potenciales (20%). Mecanismos minoritarios fueron la inducción del CYP3A4 por los tratamientos concomitantes (4,5%) y la activación de los receptores androgénicos (2,2%). Las tres interacciones más graves fueron con silodosina (sustrato de la glicoproteína-P), dexametasona y primidona (ambos inductores del CYP3A4, enzima metabolizadora de abiraterona). En la tabla 1 se detallan por orden decreciente de frecuencia los fármacos implicados en cada uno de los mecanismos y cuales serían las recomendaciones en función de la relevancia clínica de la interacción.
La distribución de las recomendaciones generales que se establecieron fue: 39,5% consistían en monitorizar estrechamente la terapia con abiraterona, 32,6% recomendaban indistintamente tanto la monitorización estrecha como la sustitución por una alternativa terapéutica disponible, 18,6% sugerían únicamente la elección de una alternativa terapéutica y 9,3% recomendaban evitar la asociación de los fármacos implicados siempre que fuera posible.
Discusión
Que las IF son una fuente de eventos adversos es un hecho ampliamente demostrado. En el estudio realizado por Ibáñez et al. se estimó que las interacciones farmacológicas son el origen del 14-25% de las reacciones adversas a medicamentos de pronóstico grave, y la causa de hospitalización del 1,6% del total de ingresos hospitalarios10. Los antineoplásicos orales son un grupo de fármacos en los que puede presentarse este problema, sobre todo en pacientes oncológicos polimedicados donde la posibilidad de sufrir una IF crece exponencialmente cuanto mayor sea el número de fármacos que tomen. Según Rentero Redondo et al. un 44% de todos los pacientes en tratamiento con antineoplásicos orales presentaron al menos 2 IF11. En nuestra población, el porcentaje de pacientes con 2 o más interacciones potenciales asciende al 67,57%, valor muy superior al estudio previo. Principalmente puede ser debido a que el presente estudio se refiere a un único fármaco destinado a tratar una patología muy prevalente en pacientes con edad avanzada en los que la polimedicación es habitual.
Tan importante es cuantificar el número de las IF potenciales como conocer la gravedad o el grado de repercusión clínica de las mismas. En la población estudiada, más del 70% de las IF detectadas son de pronóstico leve sin una evidencia clara de la aparición de clínica asociada. Dichos resultados están en concordancia con los obtenidos por estudios similares11.
Cabe destacar que los fármacos prescritos para el tratamiento sintomatológico del cáncer de próstata son causantes de un elevado porcentaje de las interacciones detectadas. Fármacos para el control del dolor como morfina, tramadol, oxicodona o fentanilo son responsables del 23,35% del total de interacciones registradas. Es recomendable por ello en los casos que sea posible realizar el control analgésico con alternativas terapeúticas libres de interacción (como podría ser tapentadol), o realizar un seguimiento estrecho del paciente con el fin de asegurar que la analgesia actúa convenientemente y sin producir efectos indeseables.
Merecen una especial mención por su potencial trascendencia las interacciones generadas por fármacos inductores del citocromo CYP3A4, del cual es sustrato abiraterona. Una interacción de este tipo puede disminuir las concentraciones plasmáticas del fármaco antiandrógeno hasta niveles infraterapéuticos. Exponentes a este nivel son las interacciones detectadas con dexametasona y primidona, que aunque no está estudiada su relevancia clínica, se ha visto una modificación relevante en la farmacocinética de abiraterona por lo que se recomienda evitar su administración conjunta o usar con precaución realizando una monitorización estrecha4,12.
Pese a su baja prevalencia en nuestro estudio (2,2%), se considera de especial interés la interacción potencial de abiraterona con los antagonistas de los receptores de mineralocorticoides debido a la repercusión clínica téorica que podría suponer. En el estudio publicado por Richards et al. en 2012 se observó que tanto espironolactona como eplerenona pueden disminuir la eficacia de abiraterona, ya que in vitro se ha demostrado una activación tanto de los receptores de andrógenos mutados como nativos13. Además de los estudios in vitro, hay publicado un caso por Sundar et al. en el que se diagnosticó falsamente de progresión bioquímica a un paciente en tratamiento concomitante con abiraterona y espironolactona. Después de una semana de tratamiento con espironolactona, el paciente experimentó un aumento sustancial del antígeno prostático específico (95 a 205 mcg/L), valor que fue revertido a sus niveles basales tras dos semanas de la suspensión de espironolactona14.
Aunque abiraterona haya demostrado en estudios pivotales y post autorización un perfil de seguridad muy aceptable, su capacidad de inhibir mútiples enzimas le hace ser un fármaco en el que no hay que menospreciar las consecuencias o eventos adversos relacionados con interacciones farmacológicas en las que puede estar implicado. Este trabajo intenta aportar, de forma resumida, la relevancia y la recomendación farmacoterapéutica ante cada interacción en base a la evidencia clínica disponible actualmente. Aunque hay que asumir que algunos de estos usos concomitantes no siempre son evitables, deben tenerse presentes a la hora de realizar la prescripción y la valoración del paciente en cuanto a signos y síntomas que alerten sobre la repercusión clínica de una interacción potencial.
Una limitación del presente estudio es que solamente se han registrado interacciones teóricas. Sería conveniente la realización de estudios posteriores que determinaran qué porcentaje de todas ellas se convierten en interacciones reales con repercusión clínica significativa.
Conclusiones
Ante los resultados obtenidos podemos concluir que la mayor parte de los pacientes incluidos en el estudio presentaron al menos una interacción potencial entre su tratamiento domiciliario y abiraterona. Más del 90% de las interacciones serían manejables con una monitorización más estrecha o con ajustes de dosis, sin conllevar un cambio de tratamiento. Principalmente se deben al efecto inhibidor de abiraterona sobre múltiples vías de metabolización.
Es aconsejable un seguimiento farmacoterapéutico estrecho y continuo de los pacientes tratados con abiraterona para detectar y manejar posibles interacciones y futuras complicaciones derivadas de ellas.
Conflicto de intereses: Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
- Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, Mathers C, et al. GLOBOCAN 2012 v1.0, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11. 2013. 2014. [citado 15 abril 2015]. Disponible en: http://www.seom.org/seomcms/images/stories/recursos/Las_cifras_del_cancer_2014.pdf.
- Reid AH, Attard G, Danila DC, Oommen NB, Olmos D, Fong PC, et al. Significant and sustained antitumor activity in post-docetaxel, castration-resistant prostate cancer with the CYP17 inhibitor abiraterone acetate. J Clin Oncol. 2010;28(9):1489-95.
- Pal SK, Sartor O. Phase III data for abiraterone in an evolving landscape for castration-resistant prostate cancer. Maturitas. 2011;68(2):103-5.
- Ficha técnica de Zytiga®. [citado 15 abril 2015]. Disponible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002321/WC500112858.pdf.
- Kasimis B, Wilding G, Kreis W, Feuerman M, Chang V, Hwang S, et al. Survival of patients who had salvage castration after failure on bicalutamide monotherapy for stage (D2) prostate cancer. Cancer Invest. 2000;18(7):602-8.
- Flores J, Armijo JA, Mediavilla A. Farmacología Humana. 5º Edición ed.: Masson-Salvat; 2008.
- Blower P, de Wit R, Goodin S, Aapro M. Drug–drug interactions in oncology: why are they important and can they be minimized? Crit Rev Oncol Hematol. 2005;55(2):117-42.
- Sánchez E, Arco Y. Revisión de las interacciones farmacológicas de los fármacos antineoplásicos orales dispensados en un servicio de farmacia. Farm Hosp. 2014;38(4):338-63.
- Serrano JI. Interacciones farmacológicas de los nuevos antirretrovirales. Farm Hosp. 2011;35(1):36-43.
- Ibáñez A, Alcalá M, García J, Puche E. Interacciones medicamentosas en pacientes de un servicio de medicina interna. Farm Hosp. 2008;32(5):293-7.
- Rentero L, Garrido MR, Pérez P, Rivero S, Martin T, Gómez M. Análisis de interacciones medicamentosas entre el tratamiento oncológico oral y la medicación domiciliaria. Abst Nº 952 Farm Hosp. 2013;(Suppl 1):65-499.
- Zytiga®. FDA. Label Information. [citado 15 abril 2015]. Disponible en: http://www.accessdata.fda.gov/drugsatfda_docs/label/2012/202379s004lbl.pdf.
- Richards J, Lim AC, Hay CW, Taylor AE, Wingate A, Nowakowska K, et al. Interactions of abiraterone, eplerenone, and prednisolone with wild-type and mutant androgen receptor: a rationale for increasing abiraterone exposure or combining with MDV3100. Cancer Res. 2012;72(9):2176-82.
- Sundar S, Dickinson PD. Spironolactone, a possible selective androgen receptor modulator, should be used with caution in patients with metastatic carcinoma of the prostate. BMJ Case Rep. 2012 Feb 25;2012: 10.1136/bcr.11.2011.5238.
____
Descargar PDF: Interacciones farmacológicas y recomendaciones terapéuticas en pacientes tratados con abiraterona
Perteneciente al: VOL. 26 – Nº2 – 2016
